Đề thi thử THPT QG năm 2021 môn Hóa học online – Đề thi của Trường THPT Liễn Sơn lần 3 giúp bạn ôn tập kiến thức một cách có hệ thống thông qua hệ thống câu hỏi đa dạng. Các câu hỏi được sắp xếp từ dễ đến khó giúp bạn tiếp cận kiến thức từng bước. Đặc biệt phù hợp với những bạn đang ôn thi. Thông qua quá trình làm bài, bạn có thể nhận ra lỗ hổng kiến thức. Điều này giúp việc học trở nên chủ động hơn.
Đề thi thử THPT QG năm 2021 môn Hóa học online – Đề thi của Trường THPT Liễn Sơn lần 3
Câu 1: Cho 8,8g etyl axetat tác dụng vừa đủ với 120 ml dung dịch KOH 1M đun nóng. Sau phản ứng cô cạn dung dịch thu được bao nhiêu gam chất rắn khan ?
Câu 2: Đốt cháy hoàn toàn triglixerit X thu được x mol CO2 và y mol H2O với x = y + 4a. Nếu thủy phân hoàn toàn X thu được hỗn hợp glicerol, axit oleic, axit stearic. Số nguyên tử H trong X là:
Câu 3: Đốt cháy hoàn toàn 0,15 mol este mạch hở, no, đơn chức thu được CO2 và H2O có tổng khối lượng là 27,9g. Công thức phân tử của X là
Câu 4: Este X có công thức phân tử C2H4O2. Đun nóng 9,0 gam X trong dung dịch NaOH vừa đủ đến khi phản ứng xảy ra hoàn toàn thu được m gam muối. Giá trị của m là
Câu 5: Trong phòng thí nghiệm, khí X được điều chế và thu vào bình tam giác như hình vẽ bên. Khí X được tạo thành từ phản ứng hóa học nào dưới đây?
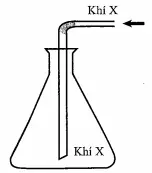
Câu 6: Thủy phân hoàn toàn 1 mol peptit mạch hở X, thu được 2 mol Gly, 2 mol Ala và 1 mol Val. Mặt khác, thủy phân không hoàn toàn X, thu được hỗn hợp các amino axit và các peptit (trong đó có Gly-Ala-Val). Số công thức cấu tạo phù hợp với tính chất của X là
Câu 7: Phát biểu nào dưới đây sai?
Câu 8: Thực hiện các thí nghiệm sau: (1) Đốt dây sắt trong khí clo. (2) Đốt nóng hỗn hợp Fe và S (trong điều kiện không có oxi). (3) Cho FeO vào dung dịch HNO3 loãng, dư. (4) Cho Fe vào dung dịch Fe2(SO4)3. (5) Cho Fe vào dung dịch H2SO4 loãng dư. Số thí nghiệm tạo ra muối sắt(II) là
Câu 9: Phát biểu nào dưới đây sai?
Câu 10: Cho các chất: NaHCO3, Ca(OH)2, Al(OH)3, SiO2, HF, Cl2, NH4Cl. số chất tác dụng với dung dịch NaOH loãng ở nhiệt độ thường là
Câu 11: Phát biểu nào dưới đây sai?
Câu 12: Cho các phát biểu sau: (a) Glucozo và saccarozo đều là chất rắn có vị ngọt, dễ tan trong nước. (b) Tinh bột và xenlulozo đều là polisaccarit. (c) Trong dung dịch, glucozo và saccarozo đều hòa tan Cu(OH)2 tạo dung dịch màu xanh lam. (d) Khi thủy phân hoàn toàn hỗn hợp tinh bột và saccarozo trong môi trường axit, chỉ thu được một loại monosaccarit duy nhất. (e) Khi đun nóng glucozo với dung dịch AgNO3 trong NH3 thu được Ag. (f) Glucozo và saccarozo đều tác dụng với H2 (Ni, ) tạo sobitol. Số phát biểu đúng là
Câu 13: Cho dãy chất sau: p-HO CH2 C6H4 OH; p-HO C6H4 COOC2H5; p-HO C6H4 COOH; p-HCOO C6H4 OH; p-CH3O C6H4 OH. Cho các điều kiện sau: (a) Chỉ tác dụng với NaOH theo tỉ lệ mol 1:1. (b) Tác dụng với Na dư tạo ra số mol H2 bằng số mol chất phản ứng. Số chất trong dãy thỏa mãn đồng thời hai điều kiện (a) và (b) là
Câu 14: Phát biểu nào sau đây đúng?
Câu 15: Phương pháp nhận biết các ion kim loại kiềm: 1. Thử màu ngọn lửa. 2. Tạo muối màu đặc trưng cho từng ion. C. Tạo kết tủa đặc trưng cho từng ion. Các phương pháp đúng là
Câu 16: Những ý kiến đúng: (1) Các oxit của kim loại kiềm phản ứng với CO tạo thành kim loại. (2) Các kim loại Ag, Fe, Cu và Mg đều được điều chế được bằng phương pháp điện phân dung dịch. (3) Các kim loại Mg, K và Fe đều khử được ion Ag+ trong dung dịch thành Ag. (4) Cho Cu vào dung dịch FeCl3 dư, thu được dung dịch chứa 3 muối.
Câu 17: Cho CO (dư) qua Al2O3, FeO, CuO ở nhiệt độ cao đến phản ứng hoàn toàn thu được chất rắn X. Để hòa tan X có thể dùng chất nào?
Câu 18: Khi không có không khí, 2 kim loại nào tác dụng với HCl theo cùng tỉ lệ số mol?
Câu 19: Nhận xét nào là đúng khi điện phân dung dịch NaCl có màng ngăn sau?
Câu 20: Dùng thêm 1 thuốc thử nào dưới đây có thể phân biệt được các dung dịch không nhãn bằng phương pháp hóa học: $AlC{l_3},\,ZnC{l_2},\,CuC{l_2},\,Fe{(N{O_3})_2},$$\,NaCl$ đựng trong các lọ mất nhãn?
Câu 21: Tính chất vật lí nào dưới đây của kim loại nhưng không phải do sự tồn tại của các eletron tự do trong kim loại quyết định?
Câu 22: Tính thành phần phần trăm khối lượng của Cu trong hỗn hợp khi cho 12 gam hỗn hợp gồm Fe, Cu tác dụng với dung dịch ${H_2}S{O_4}$ loãng thu được 2,24 lít khí ${H_2}$ (đktc).
Câu 23: Xác định tên kim loại khi cho 49,68 gam một kim loại chưa biết hóa trị tác dụng hết với dung dịch $HN{O_3}$ thu được 15,456 lít ${N_2}O$ là sản phẩm khử duy nhất (đktc).
Câu 24: Có 3 dung dịch $NaOH,\,HCl,\,{H_2}S{O_4}$ loãng. Thuốc thử duy nhất để phân biệt 3 dung dịch là
Câu 25: Đốt cháy hoàn toàn V lít hơi một amin X bằng một lượng oxi vừa đủ tạo ra 8V lít hỗn hợp gồm khí cacbonic, khí nitơ và hơi nước (các thể tích khí và hơi đều đo ở cùng điều kiện). Amin X có cùng bậc với ancol metylic. Chất X là
Câu 26: Trong bình kín chứa 40 ml khí oxi và 35 ml hỗn hợp khí gồm hiđro và một amin đơn chức X. Bật tia lửa điện để phản ứng cháy xảy ra hoàn toàn, rồi đưa bình về điều kiện ban đầu, thu được hỗn hợp khí có thể tích là 20 ml gồm 50%CO2, 25%N2, 25%O2. Coi hơi nước đã bị ngưng tụ. Chất X là
Câu 27: Cho 11,8 gam amin đơn chức X tác dụng vừa đủ với dung dịch HCl, sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Y. Làm bay hơi dung dịch Y được 19,1 gam muối khan. Số công thức cấu tạo ứng với công thức phân tử của X là
Câu 28: Đốt bao nhiêu mol hỗn hợp X gồm 2 amin no đơn chức mạch hở thu được 5,6 (l) CO2 (đktc) và 7,2 g H2O?
Câu 29: Cho 11,25 gam C2H5NH2 tác dụng với 200 ml dung dịch HCl có nồng độ bao nhiêu biết sau phản ứng xong thu được dung dịch có chứa 22,2 gam chất tan?
Câu 30: Có bao nhiêu đp thõa mãn biết ta đốt cháy một amin no đơn chức mạch hở X ta thu được CO2 và H2O có tỉ lệ mol nCO2 : nH2O = 8:11. Biết rắng khi cho X tác dụng với dung dịch HCl tạo muối RNH3Cl.
Câu 31: Đốt 2 amin no, đơn chức thu được VCO2 : VH2O = 8 : 17. Công thức của 2 amin là gì?
Câu 32: Cho 13,35 gam X gồm 2 amin no vào HCl chứa 22,475 gam muối. Nếu đốt 13,35 gam hỗn hợp X thì trong sản phẩm cháy có VCO2 : VH2O bằng bao nhiêu?
Câu 33: Có 2 amin bậc 1: (A) là đồng đẳng của anilin, (B) là đồng đẳng của metylamin. Đốt 3,21g (A) thu được 336 ml N2 (đktc). Khi đốt (B) thì VCO2 : VH2O = 2 : 3. CTCT của (A),(B) lần lượt là gì?
Câu 34: Điều không đúng về X nếu X thõa mãn cho 0,9 gam 1 amin đơn chức X cần vừa đủ với 200 ml dung dịch H2SO4 có pH = 1
Câu 35: Cho A là hợp chất hữu cơ mạch vòng chứa C, H, N trong đó có 15,054%N tác dụng với HCl tạo ra muối có dạng RNH3Cl. Cho 9,3g A tác dụng hết với nước brom dư thu được bao nhiêu gam kết tủa?
Câu 36: Dãy kim loại phản ứng với nước tạo ra môi trường bazơ?
Câu 37: Cho CO dư qua CuO, Al2O3 và MgO (nung nóng) thu được chất rắn gì?
Câu 38: Cho Al, Fe, Cu và ZnSO4, AgNO3, CuCl2, MgSO4 thì kim loại nào tác dụng được tất cả chất đã cho?
Câu 39: Để phát hiện rượu (ancol etylic) trong hơi thở của các tài xế một cách nhanh và chính xác, cảnh sát dùng một dụng cụ phân tích có chứa bột X là oxit của crom và có màu đỏ thẫm. Khi X gặp hơi rượu sẽ bị khử thành hợp chất Y có màu lục thẫm. Công thức hóa học của X là Y lần lượt là
Câu 40: Một oxit của nguyên tố R có các tính chất sau: - Tính oxi hóa rất mạnh. - Tan trong nước tạo thành hỗn hợp dung dịch H2RO4 và H2R2O7. - Tan trong dung dịch kiềm tạo anion RO42- có màu vàng. Công thức oxit của R là